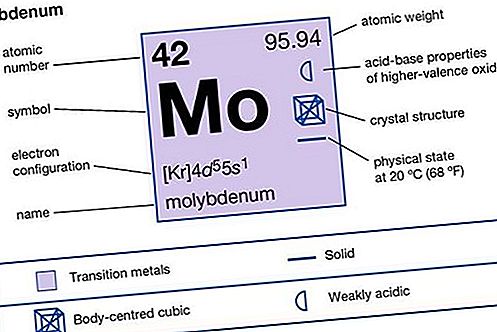
Molibden (Mo), kemični element, srebrno-siva ognjevzdržna kovina skupine 6 (VIb) periodične tabele, ki se uporablja za zagotavljanje vrhunske trdnosti jeklu in drugim zlitinam pri visoki temperaturi.
Švedski kemik Carl Wilhelm Scheele je pokazal (približno 1778), da mineral molibdaina (danes molibdenit), za katerega se je dolgo mislilo, da je svinčena ruda ali grafit, vsekakor vsebuje žveplo in morda še neznano kovino. Na predlog Scheele je Peter Jacob Hjelm, še en švedski kemik, uspešno izoliral kovino (1782) in jo imenoval molibden, iz grških molibdov, "svinec".
Molibdena v naravi ni. Sorazmerno redek element, približno tako bogat kot volfram, po katerem spominja. Za molibden je glavna ruda molibden - molibden disulfid, MoS 2 -, vendar najdemo tudi molibdate, kot so svinčev molibdat, PbMoO 4 (wulfenit) in MgMoO 4. Večina komercialne proizvodnje je iz rud, ki vsebujejo mineral molibdenit. Koncentrirani mineral je običajno pražen v presežku zraka, da dobimo molibdenov trioksid (MoO 3), imenovan tudi tehnični molibdijev oksid, ki ga lahko po čiščenju reduciramo z vodikom do kovine. Naknadno zdravljenje je odvisno od končne uporabe molibdena. Molibdenu se lahko doda jeklo v peči v obliki tehničnega oksida ali feromolibdena. Ferromolibden (ki vsebuje vsaj 60 odstotkov molibdena) nastane z vžigom mešanice tehničnega oksida in železovega oksida. Molibden kovina se proizvaja v obliki praška z redukcijo z vodikom kemično čiste molibdenovega oksida ali amonijevega molibdata, (NH 4) 2 MoO 4. Prah se pretvori v masivno kovino s postopkom metalurške prahu ali s postopkom vlivanja obloka.
Zlitine na bazi molibdena in sama kovina imajo koristno trdnost pri temperaturah, nad katerimi se stali večina drugih kovin in zlitin. Najpomembnejša uporaba molibdena pa je kot legirno sredstvo pri proizvodnji železnih in neželeznih zlitin, h kateremu edinstveno prispeva vroča trdnost in odpornost proti koroziji, npr. Je eden najučinkovitejših elementov za večjo utrjenost železa in jekla, poleg tega pa prispeva k žilavosti kaljenih in kaljenih jekel. Visoka korozijska odpornost, potrebna za nerjavna jekla, ki se uporabljajo za predelavo farmacevtskih izdelkov in kromovih jekel za avtomobilske obloge, je edinstveno povečana z majhnimi dodatki molibdena. Kovinski molibden se uporablja za električne in elektronske dele, kot so nosilci nitk, anode in rešetke. Palica ali žica se uporablja za ogrevanje elementov v električnih pečeh, ki delujejo do 1.700 ° C (3.092 ° F). Prevleke iz molibdena se trdno oprijemajo jekla, železa, aluminija in drugih kovin ter kažejo odlično odpornost proti obrabi.
Molibden je precej odporen proti napadom s kislinami, razen mešanic koncentrirane dušikove in fluorovodikove kisline, hitro pa ga lahko napademo z alkalno oksidacijskimi talinami, kot sta zlitina kalijevega nitrata in natrijevega hidroksida ali natrijevega peroksida; vodne alkalije pa so brez učinka. Pri normalni temperaturi je inerten za kisik, vendar se z njim zlahka kombinira pri rdeči vročini, da daje triokside, pri sobni temperaturi pa ga napada fluor in daje heksafluoride.
Naravni molibden je mešanica sedmih stabilnih izotopov: molibden-92 (15,84 odstotka), molibden-94 (9,04 odstotka), molibden-95 (15,72 odstotka), molibden-96 (16,53 odstotka), molibden-97 (9,46 odstotka), molibden-98 (23,78 odstotka) in molibden-100 (9,13 odstotka). Molibden ima oksidacijsko stanje od +2 do +6 in se šteje, da prikazuje ničelno oksidacijsko stanje v karbonilni Mo (CO) 6. Molibden (+6) se pojavlja v trioksidu, najpomembnejši spojini, iz katere je pripravljena večina drugih spojin, in v molibdatih (ki vsebujejo anion MoO 4 2−), ki se uporabljajo za proizvodnjo pigmentov in barvil. Molibden disulfid (MoS 2), ki spominja na grafit, se uporablja kot trdno mazivo ali kot dodatek maščobam in olji. Molibden tvori trde, ognjevzdržne in kemično inertne intersticijske spojine z borom, ogljikom, dušikom in silicijem ob neposredni reakciji s temi elementi pri visokih temperaturah.
Molibden je bistven element v sledeh v rastlinah; v stročnicah kot katalizatorju pomaga bakterijam pri določanju dušika. Kot mikrohranila sta bila uporabljena molibdenov trioksid in natrijev molibdat (Na 2 MoO 4).
Največji proizvajalci molibdena so Kitajska, ZDA, Čile, Peru, Mehika in Kanada.
Lastnosti elementov
| atomsko število | 42 |
|---|---|
| atomska teža | 95,94 |
| tališče | 2610 ° C |
| vrelišče | 5.560 ° C (10.040 ° F) |
| specifična težnost | 10,2 pri 20 ° C (68 ° F) |
| oksidacijska stanja | 0, +2, +3, +4, +5, +6 |
| konfiguracija elektronov | [Kr] 4d 5 5s 1 |