Določitev značilnosti
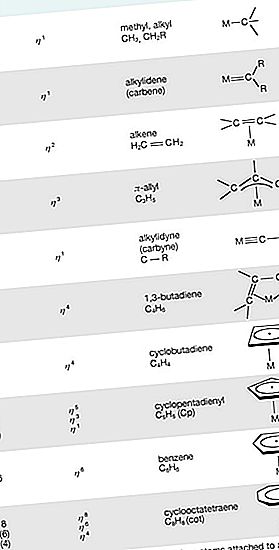
Spojina velja za organometalno, če vsebuje vsaj eno vez kovina-ogljik (M ― C), pri čemer je ogljik del organske skupine. Običajno organska skupina vsebuje vezi ogljik-vodik (C-H); na primer, z lahkoto metilno skupino, CH 3, in večji homologov, kot so etil skupino, C 2 H 5, ki se veže na kovinski atom hrbet samo enim ogljikovim atomom. (Simple alkilnih skupin, kot so te pogosto okrajšana s simbolom R.), bolj izpopolnjen organske skupine vključujejo skupino ciklopentadienil, C 5 H 5, v katerem lahko vseh pet atomov ogljika tvori vezi s kovinskim atomom. Izraz kovina se v tem kontekstu razlaga široko; tako, če so organske skupine pritrjene na metaloide, kot so bor (B), silicij (Si), germanij (Ge) in arzen (As), se dobljene spojine štejejo za organometalne, skupaj s tistimi, ki vsebujejo prave kovine, kot je litij (Li), magnezij (Mg), aluminij (Al) in železo (Fe). „Kovina“ v organometalni spojini lahko vključuje večino elementov, razen dušika (N) in fosforja (P) v skupini 15 in vseh elementov v skupinah 16 (kisikova skupina), 17 (halogeni) in 18 (žlahtni plini).
Primer organokovinsko spojino je trimethylboron, B (CH 3) 3, ki vsebuje tri B-C vezi.
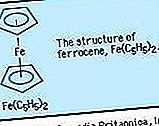
Drug razlog je ferocen, Fe (Ci 5 H 5) 2, ki ima bolj izpopolnjen strukturo z atomom železa stisnjena med dvema C 5 H 5 plošč. Nekatere spojine s kovinsko-ogljikovimi vezmi se ne štejejo za organske kovine, ker sestavni ogljikov atom ni del organske skupine; dva primera sta kovinska karbida - na primer Fe 3 C, trda trdna snov, ki je sestavina iz litega železa - in kovinske cianidne spojine - kot je pigment globoko modre barve pruske modre barve, KFe 2 (CN) 6.
Zgodovinski razvoj
Prva sintetična organokovinska spojina, K [PTCL 3 (Ci 2 H 4)], pripravimo danska farmacevta William C. Zeise leta 1827 in se pogosto sklicuje kot na Zeise sol. Takrat je imela Zeise nikakor določanje strukturo njegovega nove spojine, danes pa je znano, da struktura vsebuje molekule etilen (H 2 C = CH 2) povezano preko obeh ogljikovih atomov v osrednjem platine (Pt) atomom. Atina platine je prav tako vezan na tri atome klora (Cl). Kalijev ion, K +, je prisoten za uravnoteženje naboja.


Povezava atomov ogljika etilena na centralni atom platine uvršča Zeiseovo sol kot organometalno spojino. Razvoj z neposrednejšim vplivom na področje kemije je bilo leta 1849 odkrit nemški britanski kemik Edward C. Frankland o dietilzinku, H 5 C 2 ―Zn ― C 2 H 5, za katerega je pokazal, da je zelo koristen v organska sinteza. Od takrat se v organski sintezi tako v laboratorijih kot v industriji uporabljajo vse večje količine organometalnih spojin.
Naslednji mejnik v razvoju polja je bilo odkritje tetrakarbonilnikela, ki ga je nemški izobraženi britanski industrijski kemik Ludwig Mond in njegovi pomočniki leta 1890. Leta 1951 sta nemški teoretični kemik Ernst Otto Fischer in britanski kemik Sir Geoffrey Wilkinson neodvisno odkrila sendvič strukturo spojin ferocen. Njihova vzporedna odkritja so privedla do poznejšega razkritja drugih spojin z sendvič strukturami, zato sta leta 1973 Fischer in Wilkinson skupaj prejela Nobelovo nagrado za kemijo za prispevek k študiju organometalnih spojin. Od 50. let 20. stoletja je organska kovinska kemija postala zelo aktivno področje, ki ga je zaznamovalo odkrivanje novih organometalnih spojin, skupaj s podrobno strukturno in kemijsko karakterizacijo ter uporabo sintetičnih intermediatov in katalizatorjev v industrijskih procesih. Dva Organometallics pojavljale v naravi so vitamin B 12 koencim, ki vsebuje kobalt-ogljik (Co-Ci) vez, in dimethylmercury, H 3 C-HG-CH 3, ki se ga proizvaja bakterija odpraviti strupen kovinsko živo srebro. Vendar so organometalne spojine na splošno neobičajne v bioloških procesih.