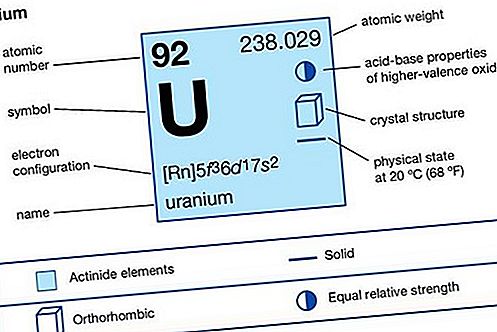
Uran (U), radioaktivni kemični element iz skupine aktinoidov periodične tabele, atomska številka 92. Je pomembno jedrsko gorivo.

aktinoidni element
člani skupine, vključno z uranom (najbolj znan), se pojavljajo v naravi, večino ljudi ustvari človek. Uporabljali smo tako uran kot plutonij
Uran predstavlja približno dva dela na milijon Zemljine skorje. Nekateri pomembni minerali urana pitchblende (nečisti U 3 O 8), uraninit (UO 2), carnotite (vanadata kalijeva urana), otunit (kalcijev urana fosfat) in torbernite (bakren uran fosfat). Te in druge obnovljive uranove rude kot viri jedrskih goriv vsebujejo mnogokrat več energije kot vsa znana obnovljiva nahajališča fosilnih goriv. En kilogram urana prinese toliko energije kot 1,4 milijona kilogramov (3 milijone funtov) premoga.
Za dodatne informacije o nahajališčih uranove rude ter o pokritju tehnik rudarjenja, rafiniranja in predelave glejte predelavo urana. Za primerjalne statistične podatke o proizvodnji urana glej tabelo.
Uran
| država | rudarska proizvodnja 2013 (metrske tone) | % svetovne proizvodnje rudnikov |
|---|---|---|
| * Oceni. | ||
| Vir: Svetovno jedrsko združenje, Svetovna proizvodnja urana (2014). | ||
| Kazahstan | 22.574 | 37.9 |
| Kanada | 9,332 | 15.6 |
| Avstralija | 6.350 | 10.6 |
| Niger * | 4,528 | 7.6 |
| Namibija | 4.315 | 7.2 |
| Rusija | 3.135 | 5.3 |
| Uzbekistan * | 2400 | 4.0 |
| Združene države | 1.835 | 3.1 |
| Kitajska * | 1.450 | 2.4 |
| Malavi | 1,132 | 1.9 |
| Ukrajina | 1,075 | 1.9 |
| Južna Afrika | 540 | 0,9 |
| Indija * | 400 | 0,7 |
| Češka | 225 | 0,4 |
| Brazilija | 198 | 0,3 |
| Romunija * | 80 | 0,1 |
| Pakistan * | 41 | 0,1 |
| Nemčija | 27 | 0,0 |
| svetovno skupno | 59,637 | 100 |
Uran je gost trdi kovinski element srebrno bele barve. Je nodularna, kovljiva in z visoko količino laka. V zraku kovina porjavi in ko se fino razdeli, razbije v plamen. Je razmeroma slab prevodnik električne energije. Čeprav ga je odkril (1789) nemški kemik Martin Heinrich Klaproth, ki ga je poimenoval po takrat nedavno odkrtem planetu Uran, je kovino prvič izoliral (1841) francoski kemik Eugène-Melchior Péligot z zmanjšanjem tetrahlorida urana (UCl 4) z kalij.
Formulacija periodičnega sistema, ki jo je leta 1869 ruski kemik Dmitrij Mendelejev osredotočil, je osredotočila pozornost na uran kot najtežji kemični element, kar je bilo vse do odkritja prvega transuranijevega elementa neptunija leta 1940. Leta 1896 je francoski fizik Henri Becquerel odkril uran pojav radioaktivnosti, izraz, ki sta ga leta 1898 prvič uporabila francoska fizika Marie in Pierre Curie. To lastnost smo pozneje našli v številnih drugih elementih. Zdaj je znano, da uran, radioaktiven v vseh njegovih izotopih, naravno sestoji iz mešanice urana-238 (99,27 odstotka, 4,510,000,000-letna razpolovna doba), urana-235 (0,72 odstotka, 713 000 000-letna razpolovna doba) in uran-234 (0,006 odstotka, 247 000-letna razpolovna doba). Te dolge razpolovne dobe omogočajo določitev starosti Zemlje z merjenjem količin svinca, uranovega končnega produkta razpada v nekaterih kamninah, ki vsebujejo uran. Uran-238 je matična in uran-234 ena od hčera v seriji razpada radioaktivnega urana; uran-235 je matična v seriji razpadanja aktinija. Glej tudi aktinoidni element.
Element uran je postal predmet intenzivnih preučevanj in širokega zanimanja, potem ko sta nemška kemika Otto Hahn in Fritz Strassmann konec leta 1938 odkrila pojav jedrske cepitve v uranu, obstreljenem s počasnimi nevtroni. Ameriški rojeni italijanski fizik Enrico Fermi je (v začetku leta 1939) predlagal, da bi lahko nevtroni spadali med produkte cepitve in bi tako lahko nadaljevali cepitev kot verižno reakcijo. Madžarski rojeni ameriški fizik Leo Szilard, ameriški fizik Herbert L. Anderson, francoski kemik Frédéric Joliot-Curie in njihovi sodelavci so to napoved potrdili (1939); pozneje Preiskava je pokazala, da je povprečje 2 1 / 2 so nevtronov na atom sprošča med cepitvi. Ta odkritja so privedla do prve samostojne jedrske verižne reakcije (2. decembra 1942), prvega preizkusa atomske bombe (16. julij 1945), prve atomske bombe, padle v vojni (6. avgusta 1945), prve atomske energije podmornica (1955), in prvi polni obseg jedrskega električnega generatorja (1957).
Fisija se zgodi s počasnimi nevtroni v relativno redkem izotopskem uranu-235 (edinem v naravi cepljivem materialu), ki ga je treba ločiti od obilnega izotopa urana-238 za različne namene. Uran-238 pa se po absorpciji nevtronov in negativnem beta razpadu pretvori v sintetični element plutonij, ki se cepi s počasnimi nevtroni. Naravni uran se zato lahko uporablja v pretvorniških in rejskih reaktorjih, v katerih cepitev vzdržuje redki uran-235, plutonij pa nastaja hkrati s transmutacijo urana-238. Fisilni uran-233 se lahko sintetizira za uporabo kot jedrsko gorivo iz nefisilnega torija izotopa torija-232, ki je v naravi v izobilju. Uran je pomemben tudi kot primarni material, iz katerega so s transmutacijskimi reakcijami pripravljeni sintetični transuranijevi elementi.
Uran, ki je močno elektropozitiven, reagira z vodo; raztaplja se v kislinah, ne pa v alkalijah. Pomembna oksidacijska stanja so +4 (kot v oksidu UO 2, tetrahalidi, kot je UCl 4, in zeleni vodni ion U 4 +) in +6 (kot v oksidu UO 3, heksafluoridu UF 6 in rumenem uranilu ion UO 2 2+). V vodni raztopini je uran najbolj stabilen kot uranil ion, ki ima linearno strukturo [O = U = O] 2+. Uran ima tudi stanje +3 in +5, vendar so ustrezni ioni nestabilni. Rdeči ion U 3+ se počasi oksidira tudi v vodi, ki ne vsebuje raztopljenega kisika. Barva UO 2 + ion ni znan, ker je podvržen disproporcionacija (UO 2 + se hkrati zmanjša na U 4 + in oksidiran UO 2 2+) tudi v zelo razredčenih raztopinah.
Uranove spojine so bile uporabljene kot barvila za keramiko. Uran-heksafluorid (UF 6) je trdna snov z nenavadno visokim parnim tlakom (115 torr = 0,15 atm = 15 300 Pa) pri 25 ° C (77 ° F). UF 6 je kemično zelo reaktiven, vendar se kljub njegovi jedki naravi v parnem stanju UF 6 pogosto uporablja v metodah difuzije plina in plinske centrifuge za ločevanje urana-235 od urana-238.
Orgometalne spojine so zanimiva in pomembna skupina spojin, v katerih obstajajo kovinsko-ogljikove vezi, ki povezujejo kovino z organskimi skupinami. Uranocene je organouranium Spojina U (C 8 H 8) 2, v kateri je atom urana sendvič med dvema organskimi obročnimi plasti, povezanih z cyclooctatetraene C 8 H 8. Njeno odkritje leta 1968 je odprlo novo področje organometalne kemije.
Lastnosti elementov
| atomsko število | 92 |
|---|---|
| atomska teža | 238.03 |
| tališče | 1,132,3 ° C (2070,1 ° F) |
| vrelišče | 3.818 ° C (6.904 ° F) |
| specifična težnost | 19.05 |
| oksidacijska stanja | +3, +4, +5, +6 |
| elektronska konfiguracija plinastega atomskega stanja | [Rn] 5f 3 6d 1 7s 2 |