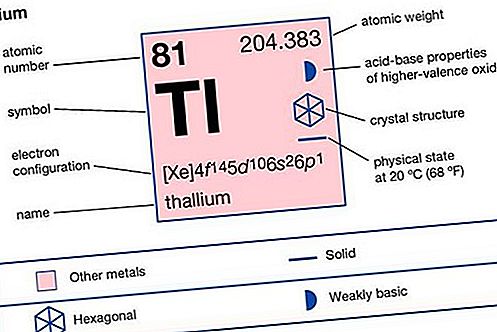
Talij (Tl), kemični element, kovina glavne skupine 13 (IIIa ali skupina bora) periodične tabele, strupen in z omejeno tržno vrednostjo. Tako kot svinec je tudi talij mehak, nizko talilni element z nizko natezno trdnostjo. Sveže rezan talij ima kovinski sijaj, ki ob izpostavljenosti zraku porjavi v modrikasto sivo barvo. Kovina ob daljšem stiku z zrakom še naprej oksidira, pri čemer nastane težka neprotektivna oksida. Talij se počasi raztopi v klorovodikovi kislini in razredči žvepleni kislini ter hitro v dušikovi kislini.

element skupine bora
(Ga), indij (In), talij (Tl) in nihonij (Nh). Kot skupina jih označujemo s tremi elektroni v najbolj oddaljenih delih
Talij, ki je redkejši od kositra, je koncentriran v le nekaj mineralov, ki nimajo tržne vrednosti. Količine talija v sledovih so prisotne v sulfidnih rudah cinka in svinca; talija se pri praženju teh rud skoncentrira v dimnih prahih, iz katerih se pridobiva.
Britanski kemik Sir William Crookes je odkril (1861) talij z opazovanjem izrazite zelene spektralne črte, nastale s piriti, ki vsebujejo selen, ki so bili uporabljeni pri izdelavi žveplove kisline. Crookes in francoski kemik Claude-Auguste Lamy sta neodvisno izolirala (1862) talij in pokazala, da gre za kovino.
Znani sta dve kristalni obliki elementa: tesno zaprti šestkotnik pod približno 230 ° C (450 ° F) in telesno usmerjen kubik zgoraj. Naravni talij, najtežji element borove skupine, je skoraj v celoti sestavljen iz mešanice dveh stabilnih izotopov: talija-203 (29,5 odstotka) in talija-205 (70,5 odstotka). Sledi več kratkotrajnih izotopov se pojavljajo kot produkti razpada v treh naravnih radioaktivnih razpadnih serijah: talij-206 in talij-210 (serija urana), talij-208 (serija torija) in talij-207 (serija aktinija).
Talijeva kovina nima komercialne uporabe in talijeve spojine nimajo večje komercialne uporabe, saj je talilni sulfat v 60. letih v veliki meri nadomeščen kot rodenticid in insekticid. Talozne spojine imajo nekaj omejene uporabe. Na primer, mešani kristali bromid-jodida (TlBr in TlI), ki oddajajo infrardečo svetlobo, so izdelani v leče, okna in prizme za infrardeče optične sisteme. Sulfida (Tl 2 S) je bil uporabimo kot osnovno sestavino v izredno občutljive fotoelektrične celice in oksisulfida v infrardečem občutljivih fotocelico (thallofide celica). Talij tvori svoje okside v dveh različnih oksidacijskih stanjih, +1 (Tl 2 O) in +3 (Tl 2 O 3). Tl 2 O se uporablja kot sestavina v visoko refrakcijskih optičnih steklih in kot barvilo v umetnih biserov; Tl 2 O 3 je polprevodnik n tipa. Kristali alkalijskih halogenidov, kot natrijev jodid, so dolirani ali aktivirani s talijevimi spojinami, da nastanejo anorganski fosforji za uporabo v scintilacijskih števcih za zaznavanje sevanja.
Talij daje plamenu bunsen plamen zeleno obarvanost. Talilni kromat s formulo Tl 2 CrO 4 je najbolje uporabiti pri kvantitativni analizi talija, potem ko je katerikoli talilni ion Tl 3+, prisoten v vzorcu, zmanjšan v stanje tala, Tl +.
Talij je značilen za elemente skupine 13, ki imajo konfiguracijo zunanjih elektronov s 2 p 1. Spodbujanje elektrona od s do ap orbitale omogoča, da je element tri ali štiri kovalenten. S talijem pa je energija, potrebna za pospeševanje s → p, visoka glede na energijo kovalentne vezi Tl – X, ki se pridobi z nastankom TlX 3; torej derivat z oksidacijskim stanjem +3 ni reakcijsko produkt, ki je zelo naklonjen energiji. Tako talij, za razliko od drugih elementov skupine bora, večinoma tvori posamično napolnjene talijeve soli, ki imajo talij v +1, ne pa v oksidacijskem stanju +3 (elektroni 6s 2 ostanejo neuporabljeni). Edini element, ki tvori stabilen enosmerno nabit kation z zunanjo konfiguracijo elektronov (n-1) d 10 ns 2, kar nenavadno ni konfiguracija inertnega plina. V vodi brezbarven, stabilnejši talonski ion, Tl +, spominja na težje ione alkalijskih kovin in srebra; spojine talija v stanju +3 se zlahka reducirajo na spojine kovine v stanju +1.
Talij v stanju oksidacije +3 spominja na aluminij, čeprav se zdi, da je ion Tl 3+ prevelik, da bi tvoril alume. Zaradi zelo podobne velikosti enkrat napolnjenega talijevega iona, Tl + in rubidijevega iona, Rb +, so številne soli Tl +, kot so kromat, sulfat, nitrati in halogenidi, izomorfne (tj. Imajo enak kristal strukturo) do ustreznih rubidijevih soli; tudi ion Tl + lahko nadomesti ion Rb + v alumah. Talij sicer tvori alum, vendar pri tem nadomesti M + ion namesto pričakovanega kovinskega atoma M 3+ v M + M 3+ (SO 4) 2 ∙ 12H 2 O.
Topne talijeve spojine so strupene. Sama kovina se spremeni v take spojine s stikom z vlažnim zrakom ali kožo. Zastrupitev s talijem, ki je lahko usodna, povzroči živčne in prebavne motnje ter hitro izgubo las.
Lastnosti elementov
| atomsko število | 81 |
|---|---|
| atomska teža | 204,37 |
| tališče | 303,5 ° C (578,3 ° F) |
| vrelišče | 1.457 ° C |
| specifična težnost | 11,85 (pri 20 ° C [68 ° F]) |
| oksidacijska stanja | +1, +3 |
| konfiguracija elektronov. | [Xe] 4f 14 5d 10 6s 2 6p 1 |