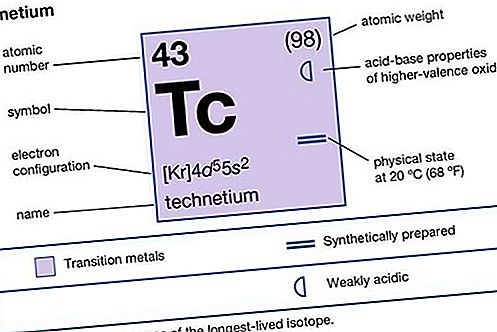
Tehnecij (Tc), kemični element, sintetična radioaktivna kovina iz skupine 7 (VIIb) periodične tabele, ki je prvi umetno proizveden. Izotop tehnecij-97 (razpolovna doba 4.210.000 let) sta leta 1937 odkrila italijanski mineralog Carlo Perrier in ameriški fizik Emilio Segrè, rojen v Italiji, v vzorcu molibdena, ki so ga bombardirali z deuteroni v Berkeleyju (Kalifornija) ciklotrona. Ta izotop je najdlje živi član skupine tehnecij-85 do tehnecij-114, ki je bil od takrat proizveden. Najpomembnejši izotop, ker je edini na voljo v velikem obsegu, je tehnecij-99 (razpolovna doba 211.000 let); proizvaja se v kilogramskih količinah kot produkt cepitve v jedrskih reaktorjih. Kovina Technetium je videti kot platina, vendar se običajno dobi kot prah sive barve. Kristalizira v šesterokotni zaprti strukturi in je superprevodnik pod 11,2 K. Razen tehnecij-99, tehnecij-97 in tehnecij-98 (4.200.000-letna razpolovna doba) so izotopi tehnecija kratkotrajni. Metastabilni izotopski tehnecij-99m (6-urna razpolovna doba), ki se uporablja z radiografskimi napravami za skeniranje, je dragocen za preučevanje anatomske strukture organov. Technetium se uporablja tudi kot metalurški sledilnik in v korozijsko odpornih izdelkih.
Tehnecij se pojavlja v Zemljini skorji kot minljive sledi spontane cepitve urana; sorazmerno kratka razpolovna doba izključuje obstoj kakršnega koli prvotnega tehnecija na Zemlji. Odkritje ameriškega astronoma Paul W. Merrill iz leta 1952, da je tehnecij-99 prisoten v zvezdah tipa S, je bilo dragocen dokaz o evoluciji zvezd in nukleosintezi. Tehnecij, kemično podoben reniju (atomska številka 75), obstaja v oksidacijskih stanjih +7, +6 in +4 v spojinah, kot so kalijev pertehnetat, KTcO 4, tehnecijev klorid, TcCl 6 in tehnecijev sulfid, TcS 2.. Spojine so znane v vseh formalnih oksidacijskih stanjih od -1 do +7.
Lastnosti elementov
| atomsko število | 43 |
|---|---|
| najpogostejši izotop | (99) |
| tališče | 2.172 ° C (3.942 ° F) |
| vrelišče | 4.877 ° C (8.811 ° F) |
| specifična težnost | 11,5 (20 ° C) |
| oksidacijska stanja | +4, +6, +7 |
| konfiguracija elektronov. | [Kr] 4d 6 5s 1 |