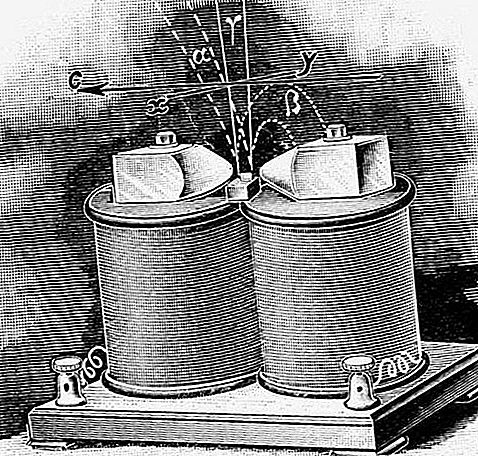
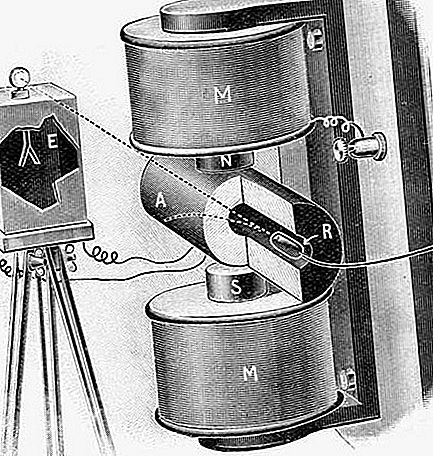
Radij (Ra), radioaktivni kemični element, najtežja zemeljsko-zemeljska kovina skupine 2 (IIa) periodične tabele. Radij je srebrno bela kovina, ki se v naravi ne pojavlja brezplačno.
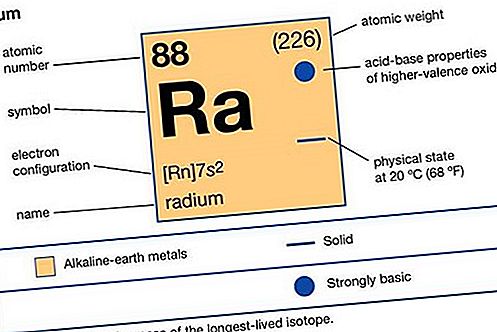

zemeljsko-zemeljske kovine
barij (Ba) in polmer (Ra).
Lastnosti elementov
| atomsko število | 88 |
|---|---|
| najbolj stabilen izotop | 226 |
| tališče | približno 700 ° C (1300 ° F) |
| vrelišče | ni dobro uveljavljen (približno 1.100–1.700 ° C [2.000–3.100 ° F]) |
| specifična težnost | približno 5 |
| oksidacijsko stanje | +2 |
| konfiguracija elektronov | [Rn] 7s 2 |
Pojav, lastnosti in uporabe
Radij so odkrili Pierre Curie, Marie Curie in pomočnik G. Bémont, potem ko je Marie Curie opazila, da je radioaktivnost smole štirikrat ali petkrat večja od tiste, ki jo vsebuje uran, in ni bila v celoti pojasnjena. osnova radioaktivnega polonija, ki jo je pravkar odkrila v ostankih smolende. Novo, močno radioaktivno snov bi lahko koncentrirali z barijem, a ker je bil njen klorid nekoliko bolj netopen, ga je mogoče oboriti s frakcijsko kristalizacijo. Ločitvi je sledilo povečanje intenzivnosti novih linij v ultravijoličnem spektru in stalno povečanje navidezne atomske teže materiala, dokler ni bila dosežena vrednost 225,2, kar je približno blizu trenutno sprejete vrednosti 226,03. Do leta 1902 smo z rafiniranjem več ton ostankov smolende pripravili 0,1 gram čistega radijevega klorida, do leta 1910 pa sta Marie Curie in André-Louis Debierne kovino izolirala.
Znanih je štiriindvajset izotopov radija, vsi radioaktivni; njihova razpolovna doba, razen radija-226 (1.600 let) in radija-228 (5.75 let), je krajša od nekaj tednov. Dolgoživi radij-226 najdemo v naravi kot rezultat njegovega nenehnega tvorjenja iz razpada urana-238. Radij se tako pojavlja v vseh uranovih rudah, vendar je širše razširjen, ker tvori vodotopne spojine; Zemljina površina vsebuje ocenah 1,8 x 10 13 g (2 x 10 7 ton) radija.
Ker so vsi izotopi radija radioaktivni in kratkotrajni na geološkem časovnem merilu, bi vsak prvotni polmer že zdavnaj izginil. Zato se radij pojavlja v naravi le kot produkt razkroja v treh naravnih sevanjih razpada (torij, uran in aktinij). Radium-226 je član serije upadanja urana. Njen starš je torij-230 in hčer radon-222. Nadaljnji produkti razpada, prej imenovani radij A, B, C, C ′, C ″, D in tako naprej, so izotopi polonija, svinca, bizmuta in talija.